微流控芯片用于卵母細胞冷凍保存的實驗研究
卵母細胞的低溫保存是輔助生殖領域的重要方法,也為優質家畜和瀕危野生動物保種提供新途徑。卵母細胞有著復雜的細胞器和超微結構,它們對外界環境的改變非常敏感,臨床上所得到的冷凍卵母細胞的復蘇率、受精率、胚胎率及分娩率還不高。
目前,常用的卵母細胞低溫保存技術是玻璃化保存。它是采用多步法將卵母細胞加入到高濃度的低溫保護劑中,然后通過冷凍載體,如開放式拉長麥管(openpulledstraw,OPS)、石英毛細管(quartzcapillary,QC)及Cryotop法等投入液氮中,以超快的冷卻速度完成玻璃化,復溫時再采用多步法洗脫保護劑。傳統的分步添加-去除保護劑的方法使細胞在不同濃度的溶液間轉移,細胞外溶液滲透壓發生階梯狀突變,卵母細胞將受到較大的滲透損傷。近年來,有學者提出運用微流控技術來進行低溫保護劑的添加和去除,使細胞外的保護劑濃度呈連續性變化,減少對細胞的滲透損傷和毒性損傷。Song等成功制作了水平三流的微流控裝置,用于添加和去除肝癌細胞的保護劑3mol/L丙二醇,結果證明經微流控技術處理后的細胞存活率比一步法高25%,比兩步法高10%。楊云等制作了用于豬卵母細胞保護劑線性添加的微流體裝置,結果表明,微流控芯片連續添加保護劑所得細胞存活率及卵裂率(92.8%,75.8%)均顯著高于一步法(59.8%,36.6%)及兩步法(76.5%,51.6%)。微流控連續法有很多種變化線型,衣星越等進一步優化了微流控連續添加并去除保護劑的線型,設計了凸型、凹型以及直線型的添加去除方式,組合出9種聯用方案用于卵母細胞保護劑的添加和去除,結果發現凹形添加-凸型去除聯用方案所得卵母細胞存活率與囊胚率與新鮮組差異最小。但是以上研究僅優化了保護劑添加和去除的過程,并未將卵母細胞進行冷凍,離卵母細胞低溫保存的臨床應用還有一定的差距。
此外,有研究者提出將細胞在微流控芯片中進行低溫保存的一體化操作。Kondo等在微流控芯片上培養HeLa、NIH3T3及MCF-7細胞,并將裝有細胞的微流控芯片和對照組培養皿在-80℃下冷凍保存,結果表明低溫保存后微流控裝置內的細胞存活率顯著高于對照組。Li等運用聚二甲基硅氧烷(PDMS)及玻璃制作了PDMS-玻璃可控溫微流控芯片,對酵母菌細胞進行低溫保存,酵母菌細胞在有溫控芯片內的存活率(74%)顯著高于無溫控芯片(27%),但與傳統保存方法所得存活率無顯著差異。Zou等將未添加保護劑的精子置于微流控芯片投入液氮保存,冷凍后的精子存活率與發育能力與對照組無顯著差異。對于卵母細胞的冷凍保存,如果將保護劑添加、冷凍保存、復溫、保護劑去除整合在一個微流控芯片上,將大大簡化實驗步驟,防止轉移過程中的細胞丟失和對細胞造成額外的機械損傷。目前關于這方面的研究還未見報道。
針對以上問題,本文首先將傳統分步添加-去除保護劑法和微流控凸型添加-凹型去除方案分別與3種冷凍載體及方法(OPS法、QC法、Cryotop法)搭配使用,對卵母細胞進行冷凍保存實驗,驗證微流控芯片添加保護劑-冷凍載體冷凍-微流控芯片去除保護劑這一整套方案的有效性;然后選擇傳熱性能較好的透明陶瓷和玻璃制作一體化芯片,將卵母細胞在一體化芯片上進行添加-冷凍-去除實驗,以冷凍保存后的細胞存活率和發育率為判斷依據,篩選出較好的方案;最后對冷凍后卵母細胞的早期凋亡情況、胞內活性氧水平和線粒體膜電位水平進行分析,考察其冷凍后的質量。本研究是微流控芯片用于卵母細胞低溫保存的全新嘗試,提出了卵母細胞低溫保存的新思路,在臨床方面將有較好的應用前景。
1材料與方法
1.1主要試劑和溶液
組織培養液(TCM199)、二甲基亞砜(DMSO)、乙二醇(EG)、蔗糖、胎牛血清(FBS)購自Gibco公司(美國)。本實驗中所用其他試劑未特殊說明均購自Sigma公司(美國)。
本實驗中用到的溶液溫度均為37℃,濃度為體積比濃度。培養液:TCM199+10%豬卵泡液+10%FBS+激素;低溫保護劑1:TCM199+7.5%EG+7.5%DMSO+20%FBS;低溫保護劑2:TCM199+15%EG+15%DMSO+20%FBS+0.4mol/L蔗糖;去除溶液1:TCM199+20%FBS+0.3mol/L蔗糖;去除溶液2:TCM199+20%FBS+0.15mol/L蔗糖。
用于檢測細胞早期凋亡水平、胞內活性氧水平以及線粒體膜電位水平的試劑盒均購自中國碧云天生物科技有限公司。
1.2豬卵母細胞的采集和體外成熟培養
自上海市嘉定區某屠宰場采集新鮮的豬卵巢,放置于37℃含有500U青鏈霉素的生理鹽水中,在1h內運回實驗室。用帶有18G針頭的5ml注射器在卵巢表面吸取直徑為2~6mm卵泡的卵泡液后注入15ml的離心管中,靜置沉淀后,在體視顯微鏡下拾取胞質均勻且表面包被3層或以上的致密卵丘細胞的卵丘卵母復合體(COCs)。洗滌后將細胞移入四孔培養板進行培養,每孔含500滋l培養液,并覆上滅菌礦物油。放入(39依0.5)℃、95%空氣、5%CO2、飽和濕度的CO2培養箱。培養42~46h后,得到M域期卵母細胞。實驗前,用0.1%透明質酸酶反復吹打以去除卵丘細胞,后用TMC199洗滌3~5次,備用。
1.3微流控芯片的制作及微混合系統的搭建
用于低溫保護劑添加和去除的微流控芯片主要由Y型流體入口通道、蛇形溶液混合通道、細胞進出通道及細胞分析腔組成。微通道橫截面的尺寸為寬100微米伊高100微米,Y型流體入口通道每條長為10mm,蛇形混合通道每條長為17mm,微通道總長約135mm。細胞分析腔的尺寸為長2000微米伊寬1000微米伊高150微米,為防止細胞在保護劑添加和去除過程中被溶液沖走,在操作腔的左右兩側各設一排柱狀障礙物,其直徑為100微米,兩障礙物間隔為50微米。
運用模塑法制作微流控芯片。首先運用AutoCAD2007設計通道后打印光刻掩膜,對掩膜進行清洗、涂膠、前烘、曝光、顯影、堅膜,得到光刻掩膜,在模具上固化處理好的PDMS預聚體,得到帶有微通道及細胞腔的PDMS基片層,將PDMS基片與PDMS蓋片用等離子氧化處理后直接貼合,進行不可逆封接,在60℃~75℃的恒溫干燥箱中加固1h,得到PDMS微流控芯片,最后使用0.6mm打孔器制作芯片進出口。
用于冷凍的芯片采用透明陶瓷及玻璃作為蓋片,與帶有通道的PDMS基片進行不可逆封接,制作一體化PDMS-透明陶瓷以及PDMS-玻璃芯片。所用透明陶瓷為氧化鋁透明陶瓷,傳熱性能較好(傳熱系數為46W/m窯K),厚度為200微米。所用玻璃為傳熱性能較好(傳熱系數為0.7~1.1W/m窯K)的玻璃,但若同樣選用200微米的玻璃,在與透明陶瓷組相同的降溫及升溫條件下容易斷裂,因此選用1mm厚的玻璃進行芯片制作。
微流控添加-去除低溫保護劑的實驗系統如圖1所示,由微注射泵/微量進樣針/微流控芯片及體視顯微鏡組成。其中微流注射泵為雙通道注射/回吸可編程注射泵。通過注射泵調節單位時間內緩沖溶液和低溫保護劑的流量來調節混合溶液的濃度變化。
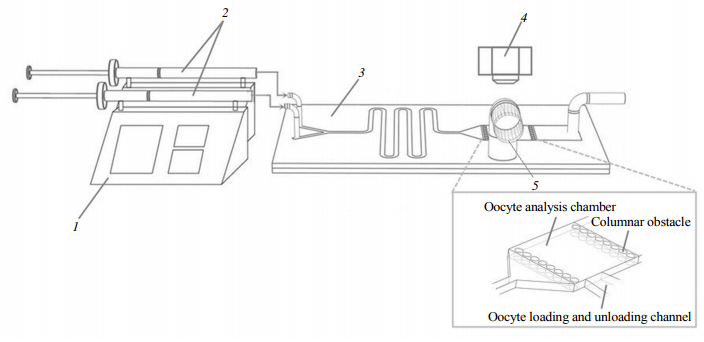
Fig.1Aschematicillustrationofthemicrofluidicexperimentalsystem1:Microinjectionpump;2:Micro-syringe;3:Y-microfluidicchip;4:Stereoscopicmicroscope;5:Oocytechannel.
1.4冷凍載體
所用OPS管參照Vajta等的制作方法,細管的內徑約為800~1000微米,壁厚約80微米。所購QC毛細管(WH-MXG-530690,蘇州汶顥微流控技術股份有限公司)制作材料為人工合成的高純度石英玻璃,其內徑為530微米,壁厚160微米。所購Cryotop,塑料薄片長20mm,寬0.4mm,厚0.1mm。
上述冷凍載體及用于冷凍的一體化芯片實物如圖2所示。

Fig.2Cryopreservationdevicesandintegrationmicrofluidicchips(a)OPS.(b)QC.(c)Cryotop.(d)PDMS-transparentceramicintegrationmicrofluidicchip.(e)PDMS-glassintegrationmicrofluidicchip
1.5實驗方法
1.5.1傳統冷凍與微流控冷凍保存方案的對比
傳統冷凍實驗分3組,每組10枚已去除卵丘細胞的M域期卵母細胞。3組細胞分別在低溫保護劑1中平衡3~5min,移入低溫保護劑2中平衡30s,加載至OPS細管、QC毛細管及Cryotop塑料薄片,隨后直接投入液氮冷凍保存。2w后將3組細胞分批次取出,含有細胞的一端迅速插入去除溶液1中,待細胞解凍后平衡5min,然后將細胞轉移至去除溶液2中平衡5min,后取出用TCM199洗滌2~3次,放入含有10%FBS的TCM199溶液中靜置1h后進行后續處理。每組實驗重復3~5次。
微流控冷凍實驗步驟如圖3a所示。實驗分3組,每組10枚已去除卵丘細胞的M域期卵母細胞,分別利用細胞口吸器放入PDMS-PDMS芯片的操作腔中,兩微量進液針內分別為低溫保護劑2和基礎液TCM199。根據衣星越等對微流控連續添加保護劑的線型優化結果,采用凹型添加法對細胞進行低溫保護劑的添加,裝有低溫保護劑2的進液針的流速變化如圖4所示,微通道內總流速為5滋l/min,總添加時間為10min。完成保護劑的添加后,用細胞口吸器將細胞吸出,迅速加載至OPS細管、QC毛細管及Cryotop塑料薄片,投入液氮進行冷凍保存。2w后將3組細胞分批次取出,含有細胞的一端放入去除溶液1中進行復溫,細胞解凍后,運用口吸器吹入細胞分析腔對3組細胞進行保護劑去除,采用凸型去除法對細胞進行保護劑的去除。兩微量進液針中分別為1mol/L的蔗糖溶液和基礎液TCM199,蔗糖溶液的流速變化如圖4所示,微通道內總流速為5滋l/min,總去除時間為8min。保護劑去除完成后將細胞吸出轉移至含有10%FBS的TCM199溶液中靜置1h后進行后續處理。每組實驗重復3~5次。
1.5.2卵母細胞一體化芯片冷凍-解凍方案
一體化芯片實驗步驟如圖3b所示。一次取6~7枚已去除卵丘細胞的M域期卵母細胞,分別利用細胞口吸器放入PDMS-透明陶瓷以及PDMS玻璃芯片的操作腔中,兩微量進液針內分別為低溫保護劑2和基礎液TCM199。然后采用與實驗1.5.1中微流控組相同的凹型添加法對細胞進行低溫保護劑的添加。完成添加后將芯片直接投入液氮進行冷凍保存2w后進行解凍處理。將芯片取出放入38.5℃的恒溫水浴中解凍,導管出口始終保持朝上,以防止液體由導管進入芯片,平衡至芯片表面沒有白霜。后選用與實驗1.5.1中微流控組相同的凸型去除法對細胞進行保護劑的去除。完成保護劑的去除后將細胞吸出轉移至含有10%FBS的TCM199溶液中靜置1h后進行后續處理。每組實驗重復3次以上。
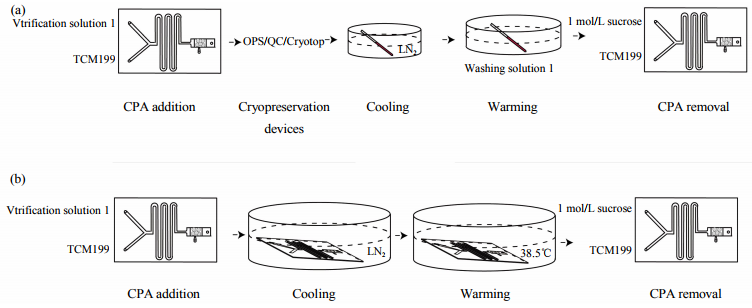
Fig.3Schematicofexperiments(a)MicrofluidicCPAaddition-removalprotocoliscombinedwiththreekindsofcryopreservationdevices.(b)Integrationmicrofluidicchipisemployedforoocytesloading,unloading,andcryopreservation.
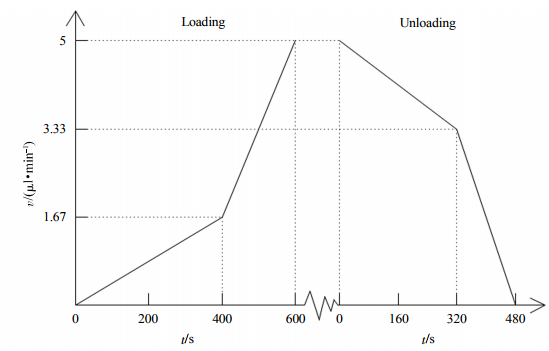
Fig.4Theflowvelocityoftheconcaveadditionwithconvexremovalcombinationprotocol
1.6卵母細胞存活率及發育率判斷
采用二乙酸熒光素(FDA)對冷凍復溫后的卵母細胞進行存活率檢測,卵母細胞用TCM199洗滌3次后轉入FDA中避光染色5~10min,再用TCM199洗滌3~5次,在倒置熒光鏡(1XY71,OLYMPUS,日本)下觀察染色情況,胞質發強熒光視為活卵,無熒光或熒光較弱為死卵。采用電激活方法對卵母細胞進行孤雌激活,使用電融合儀(Sandiego,美國)電激活卵母細胞后轉至胚胎培養液中進行培養,2d后觀察卵裂率。
1.7卵母細胞凋亡情況評價
采用Annexin吁-FITC以及PI試劑盒對冷凍復溫后的卵母細胞進行早期凋亡水平檢測。按照試劑盒的說明進行細胞染色,染色后在熒光顯微鏡下觀察細胞著色情況(Annexin吁-FITC為綠色熒光,PI為紅色熒光):正常細胞不被Annexin吁-FITC以及PI染色;凋亡早期細胞僅被Annexin吁-FITC染色,而不被PI染色;壞死或凋亡晚期細胞將同時被Annexin吁-FITC以及PI染色。統計早期凋亡細胞個數后,以早期凋亡細胞個數與總細胞個數的比值作為實驗的細胞早期凋亡率。
細胞內活性氧產生于氧化還原的中間步驟,其作用于細胞時,將引起胞內鈣離子濃度升高、能量缺失以及脂質氧化等[18]。有研究表明,冷凍保存過程中,胞內產生的活性氧會引起氧化應激、胞內基本分子退化、細胞膜的脂質氧化,從而造成卵母細胞以及胚胎的凋亡甚至死亡。采用含有熒光探針2憶,7憶-二氯熒光素二乙酸酯(2,7-dichlorofluoresceindiacetate,DCFH-DA)的活性氧檢測試劑盒對細胞進行活性氧水平檢測。染色后在熒光顯微鏡下觀察,DCFH-DA自身沒有熒光,其穿過細胞膜后,在胞內水解生成DCFH,DCFH被胞內活性氧氧化為有熒光的二氯熒光素(dichlorofluorescein,DCF),通過記錄DCF的熒光信號強度來檢測胞內活性氧水平,結果用平均熒光值表示。
線粒體在細胞中不僅僅是產生ATP的工具,在卵母細胞及胚胎的發育過程中也起著重要的作用。研究表明,在細胞的冷凍保存過程中,胞內的線粒體分布以及線粒體膜功能會發生變化,使得細胞在凍后的發育能力降低。本實驗采用線粒體膜電位檢測試劑盒(JC-1)檢測凍后細胞的線粒體膜電位。細胞染色后在激光共聚焦顯微鏡(Nikon,Japan)下觀察,當線粒體膜電位較高時,JC-1聚集在線粒體基質中,形成聚合物產生紅色熒光,當線粒體膜電位較低時,JC-1無法聚集在線粒體基質中,此時JC-1單體產生綠色熒光。通過胞內紅綠熒光比例來衡量線粒體去極化的比例,從而判斷線粒體膜電位的變化,結果用紅綠熒光強度比值的平均值表示線粒體膜電位。
1.8數據處理與分析
采用SPSSStatistics19.0對實驗結果進行分析,實驗數據用Mean依SD表示,顯著性差異標準為P<0.05。每組實驗需重復3次以上。
2結果與討論
2.1傳統冷凍與微流控冷凍保存方案對卵母細胞存活率及體外發育的影響
采用微流控添加-去除保護劑法,并與3種不同的冷凍載體搭配使用,對卵母細胞進行冷凍保存,卵母細胞的存活率和體外發育結果見表1。在QC及Cryotop中冷凍保存后,卵母細胞存活率(84.9%,89.45%)遠高于在OPS中冷凍保存(66.69%),且與對照組的存活率無顯著性差異。將不同保存方案的卵母細胞在冷凍后孤雌激活,并在培養2d后觀察卵裂率。OPS法、QC法、Cryotop法的卵裂率依次增高,為19.96%、26.58%、33.97%。
Table1Survivalratesandinvitrodevelopmentofoocytestreatedwithdifferenttraditionalandmicrofluidiccryopreservationprotocols
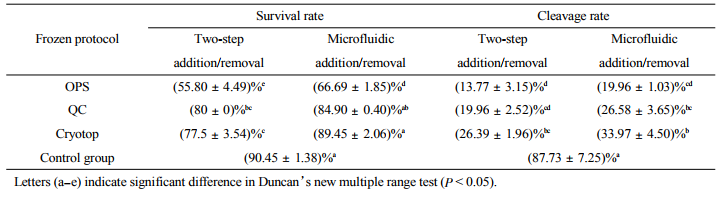
通過對比以上兩組試驗還可以發現,微流控法添加-去除保護劑與不同冷凍載體搭配冷凍后,卵母細胞存活率和卵裂率均遠高于傳統法添加-去除保護劑與對應冷凍載體搭配冷凍后的結果。說明微流控添加-去除保護劑通過控制細胞周圍的溶液濃度連續變換,減少了細胞由于保護劑濃度突然增大或減小而受到的滲透壓突變沖擊,避免了細胞體積的大幅度變化,有效減少了細胞在保護劑添加-去除時的滲透損傷。其中,微流控添加-去除保護劑搭配Cryotop載體對卵母細胞進行低溫保存得到的存活率(89.45%)與對照組的存活率(90.45%)無顯著性差異,且得到的卵裂率(33.97%)顯著高于實驗中其他冷凍方案的卵裂率。
2.2一體化微流控保存方案對細胞的存活率與體外發育的影響
卵母細胞在PDMS-透明陶瓷以及PDMS-玻璃一體化芯片低溫保存后的細胞存活率及體外發育情況,結果見表2。PDMS-透明陶瓷組的細胞存活率(59.79%)遠高于PDMS-玻璃組的細胞存活率(33.4%),將卵母細胞在冷凍后孤雌激活,并在培養2d后觀察卵裂率,PDMS-透明陶瓷組的細胞卵裂率為12.33%。實驗中PDMS-透明陶瓷以及PDMS-玻璃一體化芯片冷凍結果的不同是由于陶瓷的導熱系數(46W/m窯K)遠高于玻璃的導熱系數(0.7~1.1W/m窯K)。且選用的透明陶瓷芯片厚度為200微米,而選用的玻璃芯片厚度為1mm,傳熱阻力較大,因此PDMS-透明陶瓷芯片的保存效果優于PDMS-玻璃芯片。
Table2Survivalratesandinvitrodevelopmentofoocytestreatedwithdifferentintegratedmicrofluidiccryopreservationprotocols
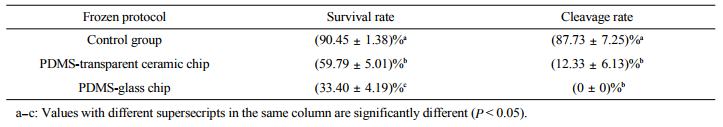
將以上結果與表1進行對比,發現PDMS-透明陶瓷組的冷凍保存與傳統添加-去除保護劑與OPS冷凍載體搭配的冷凍保存,兩者所得卵母細胞存活率(59.79%,55.80%)與卵裂率(12.33%,13.77%)無顯著性差異。但是,PDMS-透明陶瓷組的冷凍保存與傳統添加-去除保護劑與QC、Cryotop冷凍載體搭配的冷凍保存相比,卵母細胞的存活率與卵裂率均顯著低于后兩者。微流控一體化芯片的保存結果還不理想的原因在于:a。目前常用的芯片材料是PDMS,其鍵合技術、導管與芯片的密封技術都已發展成熟,但是PDMS的導熱系數較低(0.2W/m窯K),限制了其冷凍速率,從而影響玻璃化冷凍效果,目前還未找到導熱系數高且加工技術成熟的芯片材料來代替PDMS芯片。b。在操作過程中,一體化芯片在添加保護劑后沒有將多余保護劑溶液從細胞腔中移除,升降溫過程中由于細胞周圍有較多溶液覆蓋,導致升降溫速率下降
2.3微流控冷凍后卵母細胞的凋亡情況
新鮮組、微流控添加-去除法搭配Cryotop方案組以及傳統添加-去除保護劑與OPS冷凍載體組卵母細胞的早期凋亡率、活性氧水平、線粒體膜電位見表3。細胞經冷凍后,早期凋亡率顯著升高,但微流控組的卵母細胞早期凋亡率(39.44%)顯著低于傳統兩步法組(61.43%);胞內活性氧顯著升高,但微流控組的卵母細胞胞內活性氧水平(11.9)顯著低于傳統兩步法組(13.19);線粒體膜電位水平顯著降低,但微流控組的卵母細胞中線粒體膜電位水平(0.94)顯著高于傳統兩步法組(0.48)。可以看出,采用微流控法添加、去除保護劑并結合Cryotop法冷凍卵母細胞,可以有效降低卵母細胞的早期凋亡率和胞內活性氧水平,并減小線粒體損傷,提高細胞的凍后質量。
Table3Apoptosisrate,reactiveoxygenspeciesandmitochondrialmembranepotentialofoocytestreatedwithdifferentcryopreservationprotocols(n>40)

3結論
本文首先設計了用于添加-去除保護劑的微流控芯片,并首次與冷凍載體(OPS、QC、Cryotop)搭配,對卵母細胞進行冷凍保存實驗。另外為了簡化實驗步驟,首次選用玻璃及透明陶瓷作為基片制作了集CPA添加、冷凍、復溫、CPA去除為一體的透明PDMS-陶瓷、PDMS-玻璃一體化芯片并對卵母細胞進行冷凍保存。得出以下結論:
1.微流控添加-去除保護劑組卵母細胞凍后存活率以及培養后的卵裂率都顯著高于傳統添加-去除組,其中微流控添加-去除法搭配Cryotop方案的保存效果最優且可以有效降低卵母細胞的早期凋亡率和胞內活性氧水平,并減小線粒體損傷,提高細胞的凍后質量。
2.PDMS-透明陶瓷一體化芯片的卵母細胞存活率遠高于PDMS-玻璃一體化芯片,但僅與傳統添加-去除保護劑與OPS冷凍載體搭配的冷凍保存后所得卵母細胞存活率與卵裂率無顯著性差異,保存效果還不理想,在芯片材料選擇、芯片加工技術及凍存操作程序方面還有待進一步的優化。
微流控裝置搭配玻璃化冷凍載體可以有效改善保護劑添加-去除過程中細胞所受的滲透損傷和毒性損傷,提高卵母細胞的凍后存活率及質量,可作為臨床應用保存方案。另本文提出的微流控一體化芯片可以簡化實驗步驟,最大限度地減小卵母細胞受到的損傷,為卵母細胞的低溫保存提供新的思路,有廣闊的應用前景。
文獻來源生物化學DOI:10.16476/j.pibb.2018.0016作者:周新麗郭瑩瑩衣星越等(轉載僅供參考學習及傳遞有用信息,版權歸原作者所有,如侵犯權益,請聯系刪除)